|
什么是UDI医疗器械唯一标识?时间:2020-08-20 就像每个人都有对应的身份证号码一样,如今,医疗器械产品也拥有了属于自己的“身份证号码”——医疗器械唯一标识。它可以实现全链条医疗器械通查、通识,是加强全生命周期管理,提升监管效能的重要手段。 对很多人来说,医疗器械唯一标识仍是一个陌生的概念。医疗器械唯一标识由哪些部分组成?它的推广又能带来哪些好处?你了解医疗器械唯一标识吗?
医疗器械唯一标识(Unique Device Identification,缩写UDI)是美国FDA建立的”特殊医疗器械的识别系统”,是对医疗器械在其整个生命周期赋予的身份标识,是其在产品供应链中的唯一“身份证”。目前,欧美等先进国家都已经制定UDI政策法规,规定或强制要求在本国销售、流通的医疗器械上必须实施UDI标识。
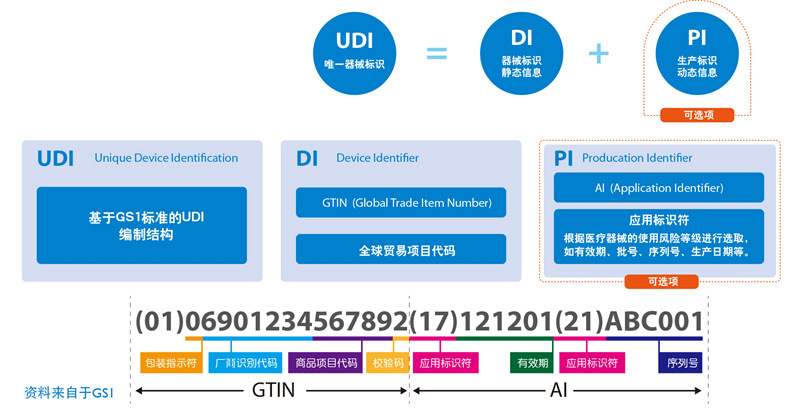
UDI标识由器械识别码(DI)和生产识别码(PI)组成。由于医疗器械产品风险和监管追溯要求的不同,其器械的UDI也随之不同。器械识别码(DI)属于静态信息,它是医疗器械产品在供应链中的身份标识,可作为进入数据库查询该产品追溯基本信息的“关键字”;而生产识别码(PI)属于动态信息,它包括医疗器械产品的序列号、批号、生产日期和有效期等,是医疗器械产品的动态附加信息。UDI可单独由DI单独标识,也可由DI加PI联合使用标识,当器械识别码(DI)和生产识别码(PI)联合使用,可以指向特定的医疗器械产品。
全球目前认可的UDI编码机构及其编码方式。
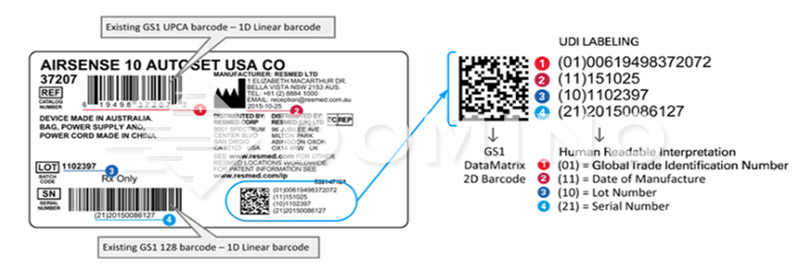
UDI标签及唯一标识数据载体UDI标签需满足两点技术要求:满足自动识别和数据采集技术(AIDC),满足人工识读(HRI)
UDI唯一标识的数据载体主要有:一维条码、二维条码和射频标签(RFID)三种形式。
2019年7月,国家药监局会同国家卫生健康委联合印发《医疗器械唯一标识系统试点工作方案》,拉开了我国UDI系统建设的序幕。到今年10月1日,列入首批实施目录的医疗器械就将正式开始实施UDI。 UDI的实施主要包括产品赋码、标识申报、数据共享与数据应用4个环节: 1、产品赋码 医疗器械注册人/备案人应按照系统规则和相关标准,选择发码机构为产品及包装创建DI,并确定PI的组成。 按照实施进度,注册人/备案人应当在申请医疗器械注册、注册变更或者办理备案时提交DI数据。 产品进入生产环节后,注册人/备案人应选择适当的载体形式,将UDI信息赋予产品的本体或其包装上。 2、标识申报 产品上市销售前,注册人/备案人须将DI和相关信息上传至UDI数据库,并负责数据的动态维护,确保DI数据的真实、准确与完整。 3、数据共享 UDI数据库通过多种方式将DI数据共享给经营企业、医疗机构、政府相关部门及社会公众。 4、数据应用 DI与PI信息联合使用,可实现医疗器械在流通和使用环节的精确识别和记录。 为什么要建立UDI系统? UDI与数据载体、数据库共同组成UDI系统。建立UDI系统,将实现六大好处。 好处一:有助于提升企业信息化管理水平,建立产品追溯体系,提升企业管理效能,助推医疗器械产业高质量发展。 好处二:有助于流通企业建立现代化物流体系,实现医疗器械供应链的透明化、可视化、智能化。 好处三:有助于医疗机构加强医疗器械在临床使用环节的风险管控,降低器械使用差错,保障患者用械安全。 好处四:有助于医疗器械监管部门构建器械监管大数据,实现对医疗器械来源可查、去向可追、责任可究,实现智慧监管。 好处五:有助于提升卫生、医保、海关等部门对于医疗器械临床使用、招标采购、医保结算、进口通关等环节的管理效率。 好处六:有助于社会公众放心用械、明白消费。 UDI系统将推动实现医疗器械智慧监管与社会共治,助力产业转型升级和健康发展,为公众提供更加安全高效的医疗服务,增强人民群众的获得感和安全感。 更多UDI赋码问题,欢迎致电依玛仕青岛服务专线0532-80928335. 山东喷码设备 青岛喷码机厂家依玛仕青岛进口喷码机,多米诺,Linx领新,依玛士、喜多力、伟迪捷等进口喷码机厂家直销,进口喷码机油墨溶剂、喷码机耗材配件,喷码机维修等业务。 |










 鲁公网安备37021402001065号
鲁公网安备37021402001065号